一、报告摘要
瀛瑞医药近日完成了CNSI-Fe单臂单药瘤内注射临床研究的中期整理与综合分析。基于53例可分析患者的现阶段数据,公司从注射病灶RECIST、全身RECIST、总体生存(OS)、基线肿瘤负荷及出组后后续治疗等多个维度进行了系统评估。
中期结果显示:
◇ CNSI-Fe单药已在人体内显示出明确且具有临床相关性的抗肿瘤活性
◇ 无论按注射病灶RECIST还是按全身RECIST评估,达到疾病控制(DCR)的患者,其后续总体生存均明显优于疾病进展(PD)患者
◇ 在随访时间超过12个月的38例患者中,全身RECIST DCR组12个月存活比例为66.7%(12/18),PD组为10.0%(2/20),另有1例患者评估NE
◇ DCR患者不仅生存结局更优,而且进入后续治疗更晚,提示其临床获益持续时间相对更长
公司认为,上述结果表明,CNSI-Fe已完成创新抗肿瘤项目最关键的一步:从机制成立走向人体有效。这为后续重点适应症开发、联合治疗推进及项目价值重估奠定了重要基础。
二、项目背景:CNSI-Fe的开发价值正在逐步清晰
CNSI-Fe为瀛瑞医药正在推进研发的瘤内注射抗肿瘤候选药物。其特点在于:
◇ 直接注射于肿瘤病灶内
◇ 以局部肿瘤微环境重塑和肿瘤杀伤为起点
◇ 预期首先表现为注射病灶控制、中心坏死转化、肿瘤增长减缓
◇ 随后再观察是否能够转化为整体疾病控制与生存获益
与传统静脉给药抗肿瘤药物不同,CNSI-Fe的价值不应仅以“是否迅速产生高比例PR/CR”作为唯一标准,而应综合考察:
◇ 注射病灶是否获得控制
◇ 全身肿瘤负荷是否得到延缓
◇ 患者是否获得更长的疾病稳定期和生存获益
从当前中期结果看,CNSI-Fe已经初步回答了上述关键问题。
三、安全性考察
总体耐受良好,无治疗相关死亡;
◇ 主要不良事件(AE)为局部反应,包括注射部位疼痛、发热感;
◇ 少数患者出现一过性恶心、呕吐或血清铁升高,10–15 h 内恢复;
◇ 在多次给药(Ib/IIa 期)中,未观察到累积毒性。
◇ IbIIa期加用预防性治疗后局部不良事件明显减少,由I期SAE发生率42.11%减少至IbIIa期SAE发生率11.63%。
CNSI-Fe 局部用药安全可控,主要与介入治疗相关不良事件,未发现明显的造血系统损害、肝肾功能异常、心血管毒性、神经系统或迟发性系统不良反应,而上述反应是目前化疗药物常见的不良反应,当达到重度时可能危及生命,是目前化疗的最大剂量、最佳疗效和疗程的主要限制。而纳米炭铁的上述不良反应可通过常规对症处理缓解,安全性良好,符合进一步联合治疗研究的安全性前提。
四、53例可分析患者:中期结果已形成清晰分层
本次中期分析基于53例可分析患者。研究过程中,项目团队采用了两套互补的疗效评估口径:
1. 注射病灶RECIST
用于判断被注射病灶本身是否获得控制,更直接反映药物局部作用。
2. 全身RECIST 1.1
用于判断患者整体疾病控制状态,更接近系统性临床获益的评价标准。
中期结果显示:
无论采用哪一种评估口径,DCR患者的后续OS均明显优于PD患者。
这意味着,CNSI-Fe单药的临床信号并非停留在局部影像变化层面,而已经与后续生存结局建立起明确关联。
五、关键结果一:按全身RECIST评估,DCR患者OS明显优于PD患者
在按全身RECIST评估,两组计算出中位生存时间OS:
◇ 全身RECIST DCR组(27例):12.75个月
◇ 全身RECIST PD组(26例):5.98个月
两组生存曲线及Kaplan-Meier估计结果见下图:
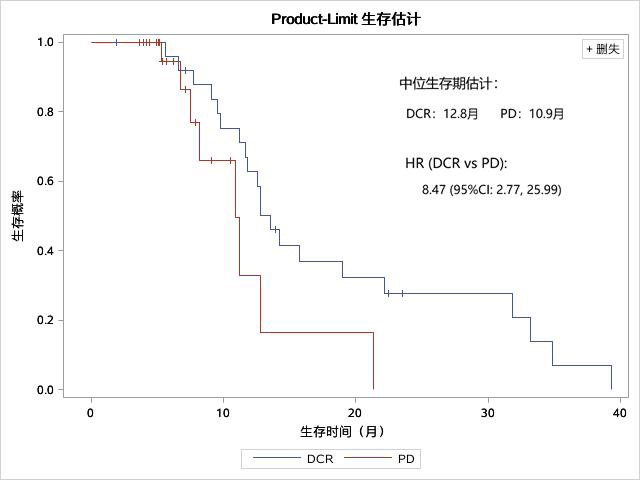
这表明:
在整体疾病控制层面,达到DCR的患者较PD患者获得了更优的后续生存结局。
这一点非常重要。因为全身RECIST反映的是患者整体病情,而不是单个病灶的局部变化。
也就是说,CNSI-Fe单药的价值不再只是“注射灶有反应”,而是已经表现出与整体临床获益相关联的信号。
按注射病灶RECIST评估,局部控制与OS改善同样相关,注射病灶RECIST DCR组(30例)和PD组(23例)中位OS分别为12.11个月和6.24个月。
这一结果说明:
注射病灶获得控制,与患者更好的后续结局存在清晰相关性。
换言之,CNSI-Fe对被注射病灶的作用并非单纯影像学现象,而具有明确临床相关性。这为项目继续推进提供了最直接的人体证据。
六、关键结果二:完成随访患者中,DCR与PD的生存分化更加明显
在随访时间超过12个月的38例患者中:
◇ 全身RECIST DCR组12个月存活比例:66.7%(12/18)
◇ 全身RECIST PD组12个月存活比例:10.0%(2/20)
这一结果表明:
达到DCR的患者,更可能获得更持久的中长期生存获益。
CNSI-Fe项目已经不再只是“有局部反应”的早期研发项目,而是在中期随访中开始出现更长期临床价值分化。
七、关键结果三:DCR患者进入后续治疗更晚,提示获益持续时间更长
在有记录患者中,DCR组与PD组在出组后治疗路径上也出现明显差异。
末次评估至启动后续治疗中位时间
◇ DCR组:41.5天
◇ PD组:27.5天
这意味着:
DCR患者不仅生存更长,而且在出组后更晚进入下一线治疗。
这类指标在肿瘤研究中非常有价值,因为它从另一个角度反映了患者临床获益的持续性。
对于项目评价而言,这说明CNSI-Fe带来的并非只是“短暂影像改善”,而更可能对应一段更具实际意义的疾病控制期。
八、结果背后的解释:DCR优势并不主要来自基线体能状态差异
基线分析显示:
◇ DCR组与PD组首次给药时ECOG评分无统计学差异
◇ 但PD组整体表现出更高的基线肿瘤负荷,包括:
· 靶病灶数目更多(平均1.8个 vs 1.4个)
· 靶病灶总尺寸更大(平均64.7cm vs 52.5cm)
· 注射病灶也略大(平均45.2cm vs 38.9cm)
这提示:
DCR组较好的结局,并不主要由基线体能状态更好所致;而更可能与更低的总体肿瘤负荷、更好的病灶控制以及更持久的疾病稳定共同相关。
这也意味着,随着后续患者筛选、病灶覆盖和联合治疗策略的进一步优化,项目临床表现仍有提升空间。
九、影像学特点提示了下一阶段最可行的开发路径
本阶段研究尚未系统获取治疗前后活检样本,因此疗效判断主要基于:
◇ CT / MRI影像变化
◇ RECIST评估
◇ OS
◇ 出组后治疗时间
◇ 临床状态变化
现有影像学观察显示:
◇ CNSI-Fe瘤内注射后,病灶中心区常可见坏死、液化或低强化改变
◇ 病灶周缘仍可见强化
这提示:
当前治疗效应可能首先集中于肿瘤中心区域,而周缘残存活性区可能构成进一步疗效放大的主要瓶颈。
同时需要特别说明的是:
◇ CNSI-Fe本身在CT上可呈高密度影
◇ 在MRI上可呈低信号
因此,治疗后影像判读必须结合:
◇ 材料本身的显影特征
◇ 中心区坏死/低强化变化
◇ 周缘强化带变化
进行综合判断,而不能机械等同于普通肿瘤自然演变。
十、从中期结果看,下一阶段最可行的策略已经逐渐清晰
基于当前53例可分析患者的中期结果,公司认为,下一阶段开发最具可行性和放大价值的路径主要有两条:
1. 尽可能覆盖全部主要靶病灶
现有数据提示,临床获益不仅取决于单个注射病灶是否被控制,也受到未覆盖肿瘤负荷明显影响。
因此下一阶段应:
◇ 尽可能提高主要肿瘤负荷覆盖率
◇ 优先纳入靶病灶数目较少、主要病灶可介入的患者
◇ 重点考虑靶病灶数目在3–5个以内的患者,以平衡覆盖率与操作可行性
2. 加快联合治疗路径开发
考虑到单靠介入技术在短期内完全解决病灶周缘覆盖问题仍有现实难度,现阶段更可行的策略是:
联合治疗 + 尽可能覆盖全部主要靶病灶
后续重点方向包括:
◇ 与放疗联合
◇ 与抗血管生成治疗联合
◇ 与免疫治疗联合
◇ 与局部热疗/近红外治疗联合
这将有助于进一步提高对病灶周缘残存活性区及未覆盖肿瘤负荷的控制能力。
十一、这份中期结果意味着什么
对纳米炭铁临床试验来说,当前最值得关注的不是单个数字,而是项目所处阶段已经发生的质变:
1.CNSI-Fe已经完成“人体有效性验证”
这使项目不再停留在前期机制叙事,而具备了更清晰的临床转化价值。
2.DCR与更优OS之间的关联已被中期结果清晰呈现
这说明项目的价值不只是局部操作层面,而是与更长期结局相关。
3.下一阶段的优化方向清楚、路径可执行
项目后续并非“方向不明”,而是已经明确聚焦在:
◇ 提高主要病灶覆盖率
◇ 优化受试者筛选
◇ 推进联合治疗开发
◇ 识别更具获益潜力的人群
4.项目的估值逻辑正在从“概念研发”转向“临床资产”
在创新药研发中,真正有价值的拐点,是从“动物或机制有效”转向“人体内已显示明确临床相关性”。
从当前中期结果看,CNSI-Fe已经进入这一阶段。
十二、结论
基于53例可分析患者的中期结果,瀛瑞医药认为,CNSI-Fe单臂单药瘤内注射研究已形成以下核心结论:
1.CNSI-Fe已在人体内显示出明确且具有临床相关性的抗肿瘤活性
2.无论按注射病灶RECIST还是按全身RECIST评估,DCR患者均较PD患者呈现更优的后续OS
3.在完成随访患者中,DCR与PD的中长期生存分化进一步加大
4.DCR患者进入后续治疗更晚,提示其临床获益持续时间更长
5.当前结果已构成CNSI-Fe单药项目的重要中期积极信号,并为后续重点适应症和联合治疗开发提供坚实基础
瀛瑞医药将继续坚持科学、审慎、规范的研发原则,稳步推进CNSI-Fe项目临床开发进程,持续提升项目临床价值与转化潜力。
十三、风险提示
本报告所述内容为基于现阶段临床研究数据开展的中期整理与分析,旨在反映项目研发进展及相关研究发现。相关结果仍需在后续更大样本研究、进一步临床验证及监管沟通中持续评估。
新药研发具有投入大、周期长、风险高等特点,项目后续研发进展、注册申报及商业化存在不确定性。敬请各方理性判断并注意相关风险。